


คือกรดชนิดหนึ่ง ที่ร่างกายมนุษย์สามารถสร้างเองได้ โดยเม็ดเลือดขาวของเรานั้น จะผลิตกรดไฮโปคลอรัสขึ้นมา เพื่อใช้ในการฆ่าเชื้อโรค ทำให้การใช้น้ำ Hypochlorous Acid ในการฆ่าเชื้อโรค มีความปลอดภัยสูง เพราะไม่ได้เป็นสารเคมีอันตราย และไม่ทำให้เกิดการแพ้ หรือการระคายเคือง
การใช้ Hypochlorous Acid นั้น ยังมีข้อจำกัดอยู่มาก ทั้งเรื่องของมาตรฐานของอุปกรณ์ที่ผลิต กระบวนการผลิต Hypochlorous Acid และด้วยอายุการเก็บรักษาที่สั้นมาก ในบทความนี้ เราจะมาพูดถึงรายละเอียดทั้งหมดค่ะ
การผลิต HOCl นั้น สามารถทำได้ 2 วิธี คือ
เมื่อเราละลายโซเดียมไฮโปคลอไรท์ หรือที่บ้านเราเรียกว่า ‘ไฮเตอร์’ กับ น้ำ จะเกิด HOCl ขึ้น ตามสมการทางด้านล่าง
NaOCl + H2O → HOCl + NaOH-
HOCl นี้ จะประกอบด้วย HCl คือ กรดไฮโดรคลอริก และ ออกซิเจน ซึ่ง อะตอมของออกซิเจน จะเป็นตัว Oxidant (ตัวฆ่าเชื้อโรค) ที่มีประสิทธิภาพสูงมาก
อย่างไรก็ตามการผลิต HOCl แบบนี้ จะไม่ค่อยได้รับการยอมรับว่าปลอดภัยมากนัก เนื่องจากเป็นการเจือจางสารเคมี อาจก่อให้เกิดการระคายเคืองหากใช้โดยตรงกับผิวหนัง
การผลิต HOCl ด้วยการ Electrolysis นี้ จะมีความปลอดภัยกับผู้ใช้ที่สูงมาก เนื่องจากจะใช้เกลือ หรือ Sodium Chlorine (Nacl) เป็นสารตั้งต้นเท่านั้น จึงไม่ทำให้เกิดการระคายเคืองที่ผิวหนัง และสามารถผลิตได้ในจำนวนมาก
กระบวนการ Electrolysis ของน้ำและน้ำเกลือ จะเกิดขึ้นดังภาพนี้
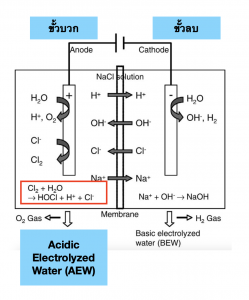
ที่ขั้วบวก เราจะได้น้ำที่เรียกว่า Acidic Electrolyzed Water (AEW) ในงานวิจัยบางงานอาจะเรียกน้ำตัวนี้ว่า Electrolyzed Oxidized Water (EOW) ซึ่งก็คือ น้ำที่ได้จากการ Electrolysis ที่ขั้วบวกนั่นเอง
คุณสมบัติของน้ำ AEW คือ มีประสิทธิภาพในการ Oxidation สูง ทำให้สามารถฆ่าเชื้อโรค เชื้อแบคทีเรียได้ สามารถวัดค่า ORP ได้ > +1000mV และมีส่วนประกอบของ Hypochlorous acid ซึ่ง HOCl นี้แหละจะมีความสามารถในการ Oxidation ที่สูงมาก
ตามคำอธิบายคือ
HOCl (hypochlorous acid)
The ions are H+, O2- and Cl+.
Chlorine attains a +1 oxidation state because Oxygen is more electronegative (so Oxygen will continue to have an oxidation state of +2).
HOCl is the answer because the chlorine in the acid reduces (gains electrons) to form Chlorine (0).
So, this is the oxizising agent because it has helped in oxidizing Cl-.
การวัดสัดส่วนว่า ในสารละลาย มี HOCl อยู่เท่าไหร่ เราจะไม่สามารถวัดเฉพาะ HOCl ได้
น้ำ Strong Acidic Electrolyzed Water ที่ออกมาเราจะไม่ได้วัดความเข้มข้นของ HOCl โดยตรง แต่จะวัดค่าที่เรียกว่า Residual Chlorine Concentration (หรืออีกชื่อหนึ่งคือ Free Chlorine) โดยสามารถวัดค่า Residual Chlorine Concentration นี้อยู่ที่ประมาณ 16 ppm
Free Chlorine นี้ จะมีสารประกอบคอรีนอยู่รวมกัน ได้แก่ Cl2, HOCl, และ OCl-
ค่า pH ของสารละลาย Electrolyzed Water จะเป็นตัวบอกว่า มีสัดส่วนของ Cl2, HOCl, OCl- อยู่มากน้อยเท่าไหร่ ตามตารางนี้ค่ะ
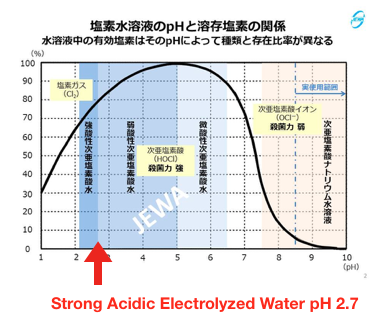
เราจะเห็นได้ว่า ช่วงที่สารละลายเป็นกรดตั้งแต่ pH 2.5 ไปจนถึง 6.5 จะเป็นช่วงของ pH ที่มี HOCl ละลายปะปนอยู่มากที่สุด
หากเราต้องการวัดความสามารถในการฆ่าเชื้อโรคของน้ำ AEW นี้ เราจะไม่ได้วัดค่า ppm ของคลอรีน ว่า ppm มากฆ่าเชื้อโรคได้มาก ppm น้อย ฆ่าเชื้อโรคได้น้อย แต่ที่เราวัดได้คือ ค่า ORP คือ ค่าความสามารถในการ Oxidation ยิ่งมากยิ่งดี ถ้าเกิน 900mV ขึ้นไป จะถือว่าฆ่าเชื้อโรคได้มีประสิทธิภาพมาก และยิ่งมีค่า ppm ของคลอรีนน้อย นั่นหมายความว่าสามารถใช้ได้อย่างปลอดภัยต่อผิวหนังมากขึ้น


ในเวปไซต์ www.jewa.org เป็นเวปขององค์กร Japan Electrolysis Water Association ได้ประกาศไว้อย่างชัดเจนว่า
ความเข้มข้นของ HOCl ที่สามารถนำมาใช้ได้อย่างปลอดภัยกับอุตสาหกรรมอาหาร (Sterilizing as food additive) จะต้องมีความเข้มข้นแค่ 10-80 ppm เท่านั้น
คำเตือน ส่วนสารละลายอื่นๆ ที่กล่าวว่าเป็น HOCl solution แต่มีความเข้มข้นมากถึง 200 ppm ไม่ใช่ Hypochlorous acid ที่ควรนำมาใช้และอาจไม่ใช่ HOCl ที่ถูกต้อง
ฟังดูแล้ว การใช้ HOCl เป็นสารที่ปลอดภัยมาก แต่ว่า จริงๆแล้ว การใช้ HOCl ก็มีข้อจำกัด และมีข้อควรระวังอยู่มาก เช่น

https://www.lenntech.com/processes/disinfection/chemical/disinfectants-sodium-hypochlorite.htm
https://www.sciencedirect.com/topics/chemistry/hypochlorous-acid
